Unidad 3
3.1.1. CONCEPTO DE ENLACE QUÍMICOS.
3.1.2. CLASIFICACIÓN DE LOS ENLACES QUÍMICOS
3.1.3. APLICACIONES Y LIMITACIONES DE LA REGLA DEL OCTETO
3.2. ENLACE COVALENTE
3.2.1. TEORÍAS PARA EXPLICAR EL ENLACE COVALENTE Y SUS ENLACES
3.2.1.1. TEORÍAS DEL ENLACE DE VALENCIA
3.2.1.2. HIBRIDACIÓN Y GEOMETRÍA MOLECULAR
3.2.1.3. TEORÍA DEL MOLECULAR ORBITAL
3.3. ENLACE IÓNICO
3.3.1. FORMACIÓN Y PROPIEDADES DE LOS COMPUESTOS IÓNICOS
3.3.2. REDES CRISTALINAS.
3.3.2.1. ESTRUCTURA
3.3.2.2. ENERGÍA RETICULAR
3.2.1.2. HIBRIDACIÓN Y GEOMETRÍA MOLECULAR
Es en particular un dato muy interesante acerca a enlaces químicos ya que habla
sobre la estructura de estos, en particular la hibridación es como si tomaras
algunos tipos de adornos y los mezclaras para crear más tipos, ejemplo si tomaras
adornos altos, delgados, bajos o anchos y combinarlos para conseguir un adorno
mediano y ancho (esto varia), en concreto a esta mezcla se los hace llamar como
los “Orbitales híbridos”
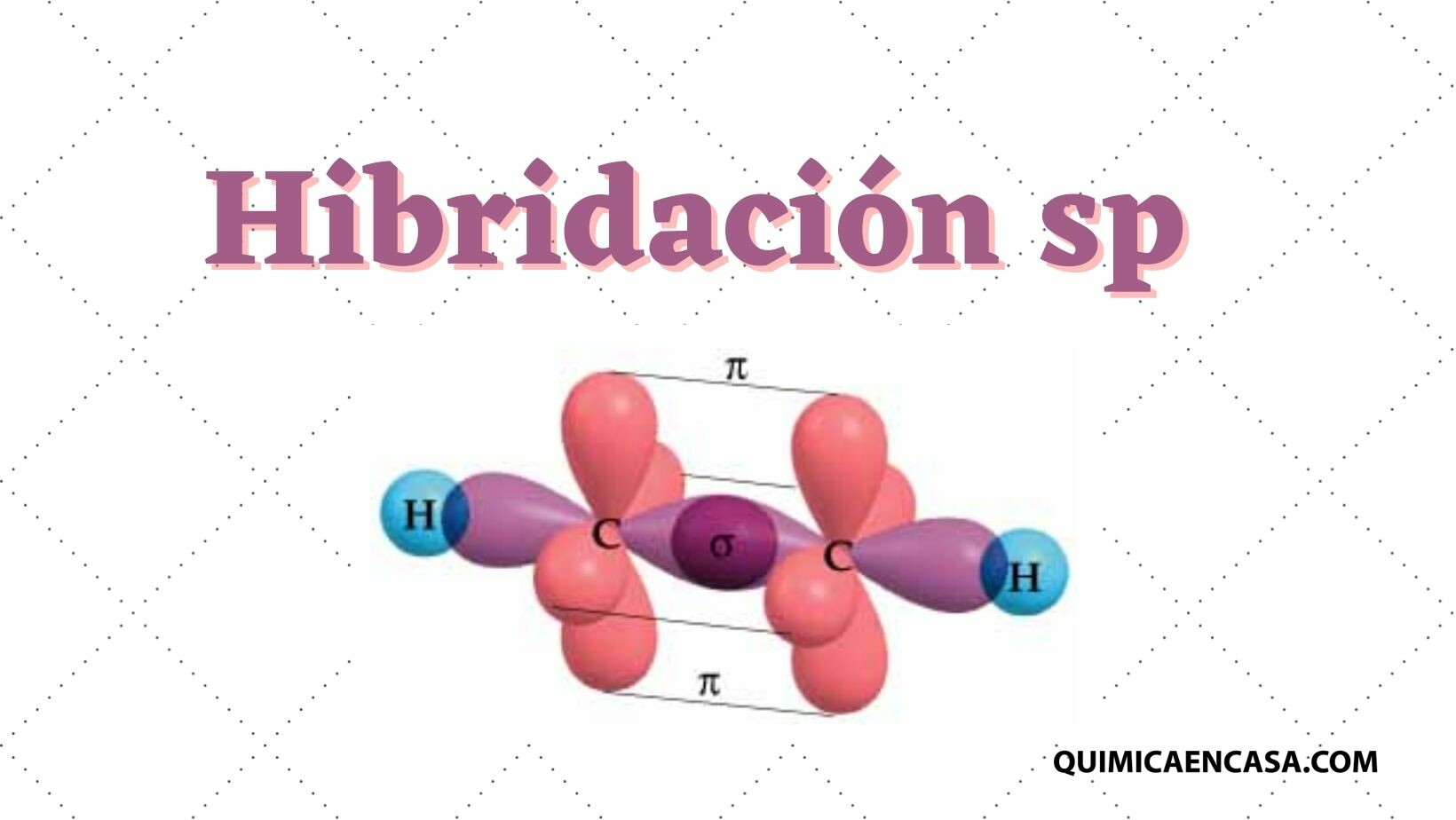
Hibridación
El concepto básico de hibridación se explica mejor en términos de la estructura del átomo de carbono, que es el elemento central en la mayoría de los compuestos orgánicos. El átomo de carbono tiene un núcleo con seis protones y usualmente seis neutrones, rodeado por seis electrones que se organizan en cuatro orbitales distintos: dos orbitales 2s y dos orbitales 2p.
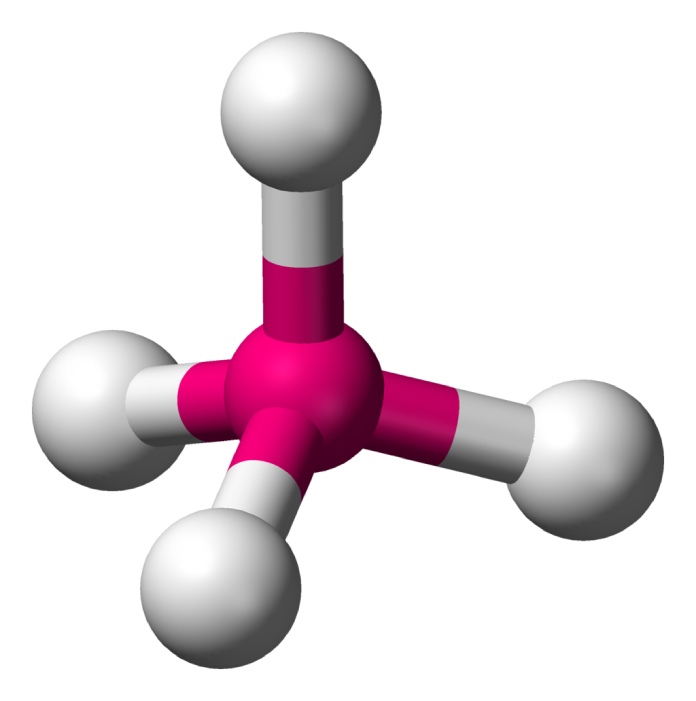
Geometría
Los compuestos orgánicos pueden tener distintos tipos de hibridación, como sp, sp2 o sp3, lo que afecta su geometría molecular y propiedades físicas y químicas. El conocimiento de la hibridación y geometría molecular permite a los químicos predecir la reactividad de los compuestos y diseñar nuevos materiales con propiedades específicas.